| 1. Introducción
5.1 Corrección déficit factores madurativos |
|
|
La anemia es un hallazgo común en el paciente quirúrgico.
Los pacientes de cirugía ortopédica mayor (COT) pueden perder más de dos litros de sangre durante el periodo perioperatorio; por ello, esta cirugía es responsable de un elevado consumo de hemoderivados. Dentro de una estrategia de ahorro de sangre es fundamental la preparación preoperatoria del paciente que incluirá el tratamiento de la anemia y la mejora de otros parámetros hematológicos, como la ferropenia, por ejemplo. El motivo fundamental es que la hemoglobina preoperatoria es el principal factor predictivo independiente de transfusión sanguínea. Por ello, debemos evitar en lo posible la anemia, corregir los estados carenciales, o bien mejorar la hemoglobina preoperatoria mediante fármacos estimulantes de la eritropoyesis, ya que existe evidencia científica suficiente de que con ello podemos reducir la exposición a sangre alogénica. |
|
|
La definición de anemia está en revisión ya que numerosos En el contexto del paciente quirúrgico, teniendo en cuenta que |
|
|
La prevalencia de anemia en los pacientes de cirugía ortopédica En cirugía ortopédica mayor, la población media que En un estudio realizado en el Hospital de la Esperanza de enero de 2001 De los pacientes estudiados, la anemia fue por déficit de nutrientes Otro aspecto destacable es la prevalencia de déficit de ácido A pesar de que los beneficios del tratamiento en este contexto no están |
|
|
Para el diagnóstico y tratamiento de la anemia preoperatoria es Es fundamental hacer una buena historia clínica que incluya los En la analítica preoperatoria de estos pacientes se debería |
|
|
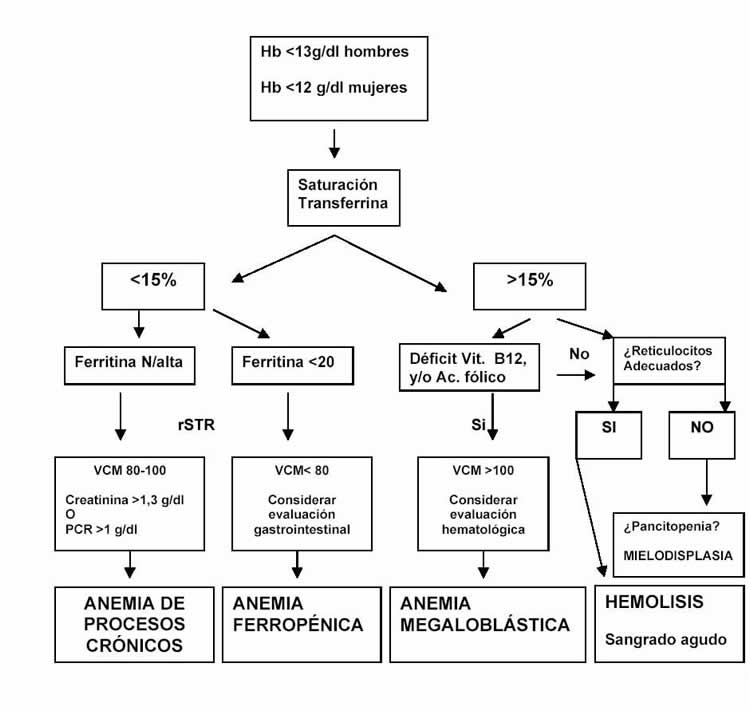
4.1. Valoración de la anemia
Hemoglobina inferior 10g/dl de causa desconocida Sí en el preoperatorio de un paciente de cirugía electiva se detecta una anemia no conocida hasta entonces o no valorada, se debe enviar el paciente al especialista que proceda, para su diagnóstico y tratamiento. Es posible que en la visita preoperatoria con la historia clínica y la analítica podamos orientar el caso.Hemoglobina inferior a 10g/dl de causa conocidaEn caso de que se trate de una anemia crónica conocida podemos intentar mejorar los parámetros hematológicos. Generalmente se trata de una anemia por proceso inflamatorio crónico acompañando a una patología de base como artritis reumatoide o una anemia por malabsorción intestinal como en la enfermedad de Crohn.Hemoglobina entre 10-13 g/dlLa anemia leve puede o no ser conocida, pero con los datos que disponemos podemos discernir como tratarla. Este grupo de pacientes junto con el anterior, son los principales candidatos a estimulación con eritropoyetina y/o a tratamiento con hierro intravenoso.No hay anemia pero sí alteración de los parámetros hematínicosEn algunos casos los pacientes tienen un déficit de ácido fólico, vitamina B12 o de hierro y aún no se ha manifestado la anemia. Si van a entrar en un programa de donación autóloga y no mejoramos estos parámetros no serán capaces de recuperar la hemoglobina tras la autodonación. Del mismo modo, si los pacientes van a perder un volumen de sangre superior al 30% de la volemia, les va a ser difícil en el postoperatorio recuperar la hemoglobina si no hemos mejorado los parámetros hematínicos, ya que la eritropoyesis precisa de hierro, fólico y vitamina B12.
|
|
|
4.3. Fisiopatología de la anemia Déficit de hierro El déficit de hierro es la causa más común de Déficit funcional de hierro El concepto de déficit funcional de hierro se ha descrito en Anemia de los procesos inflamatorios crónicos o agudos En esta última década se ha avanzado mucho en el conocimiento Anemia megaloblástica Se suele producir por déficit de ácido fólico o La principal causa de déficit de fólico es el alcoholismo El déficit de cobalamina sintomático es muy raro (<10%
|
|
|
5.1 Tratamiento déficit factores madurativos Hierro oral El tratamiento de elección es el hierro oral en los pacientes Esta contraindicado en caso de enfermedad gastrointestinal inflamatoria, La dosis recomendada es de 100-200mg/d de hierro elemental. Hierro endovenoso Las principales indicaciones del hierro endovenoso son la intolerancia Indicaciones preoperatorias de hierro intravenoso
El hierro dextrano ha sido el único tratamiento de hierro parenteral Su buena tolerancia clínica se debe a que su estructura molecular Cada vial de 5ml contiene 100 mg de hierro elemental. No se requiere dosis Los efectos secundarios son escasos y leves como dolor a la administración, La pauta que podemos utilizar para tratar la anemia ferropénica La dosis se calcula según la fórmula adjunta, aunque para Dosis Fe (mg)= peso corporal (Kg)x (Hb desada-Hb real g/L)x 0.24+depósito Normalmente monitorizamos la Hb cada semana y la ferritina a los 15- Es mejor monitorizar la administración del fármaco en Durante el tratamiento parenteral no se debe tomar hierro oral al menos 5.2 Estimulantes de la eritropoyesis Eritropoyetina La eritropoyetina humana recombinante (epoetina alfa) administrada preoperatoriamente Las pautas de tratamiento habituales son: Eritropoyetina sola (Pericirugía), si disponemos de más – 600mg/Kg (vial 40000 UI) subcutánea/semana los días Eritropoyetina sola (Pericirugía) si disponemos menos de 15 – 600mg/Kg (vial 40000 UI) subcutánea/ cada 48h (máximo Eritropoyetina como coadyuvante de la DAP, si disponemos de más – 600mg/Kg (vial 40000 UI) subcutánea/ 1 o 2 por semana, hasta Es imprescindible el tratamiento complementario con hierro oral para No debemos olvidar que si se objetiva un déficit de hierro, fólico El tratamiento preoperatorio con epoetina se tolera muy bien, ya que Hasta la fecha tampoco se ha observado aumento de las complicaciones
|
|
|
1. Shander A, Knight K, Thurer R, Adamson J, Spence 2. Rosencher N, Kerkkamp HE, Macheras G, et al. Orthopedic 3. Goodnough LT, Shander A, Spivak JL, Waters JH, Friedman 4. García-Erce JA, Solano VM, Cuenca J, Ortega 5. Salido JA, Marin CA, Gomez LA, Zorrilla P, Martin 6. Aderinto J. Brenkel IJ. Pre-operative predictors 7. Bisbe E. Tratamiento preoperatorio para el ahorro 8. Llau JV, Bisbe E. Transfusión y hemostasia. 9. Cook JD. Diagnosis and manegement of iron deficiency 10. Laupacis A and Fergusson D. Erythropoietin to minimize 11. Guralnik JM, Eisenstaedt RS, Ferrucci L, Klein 12. Beghé C, Wilson A, Ershler W. Prevalence 13. Bisbe E, Saez M, Nomen N, Castillo J. Prevalencia 14. Bisbe E, Lamsfus JA, Castillo J. Vitamin B12 deficiency 15. Andrés E, The syndrome of food-cobalamin 16. Wulffele MG, Kooy A, Lehert P, et al. Effects of 17. Bisbe E, Lamsfus JA, Castillo J, Santiveri X, Escolano 18. Carmel R, Green R, Rosenblatt DS, Watkins D. Update 19. AndresE, Loukili NH, Noel E,y col.. Vitamin B12 20. Solomon LR. Cobalamin responsive disorders in ambulatory 21. Zachee P, Chew SL, Daelemans R, Lins RL. Erythropoietin 22. Bisbe E, Sáez M, Pérez C, Castillo 23. Weiss G, Goodnough LT. Anemia of chronic disease. 24. Kaltwasser JP, Kessler U, Gottschalk R, Sucki G, 25. Bisbe E, Rodríguez C, Ruiz A, Sáez 26. Bisbe E, Castillo J, Nomen N, Mestre C, Gonzalez 27. Weber EW, Slappendel R, Hemon Y, Mahler S, Dalen 28. Karkouti K, Mc Cluskey SA; Evans L, Mahomed N, 29. Shapiro GS, Boachier AO, Dhawlikar SH, Maier LS |
|